Benzen là gì? Tính chất hóa học, cấu tạo và ứng dụng thực tiễn
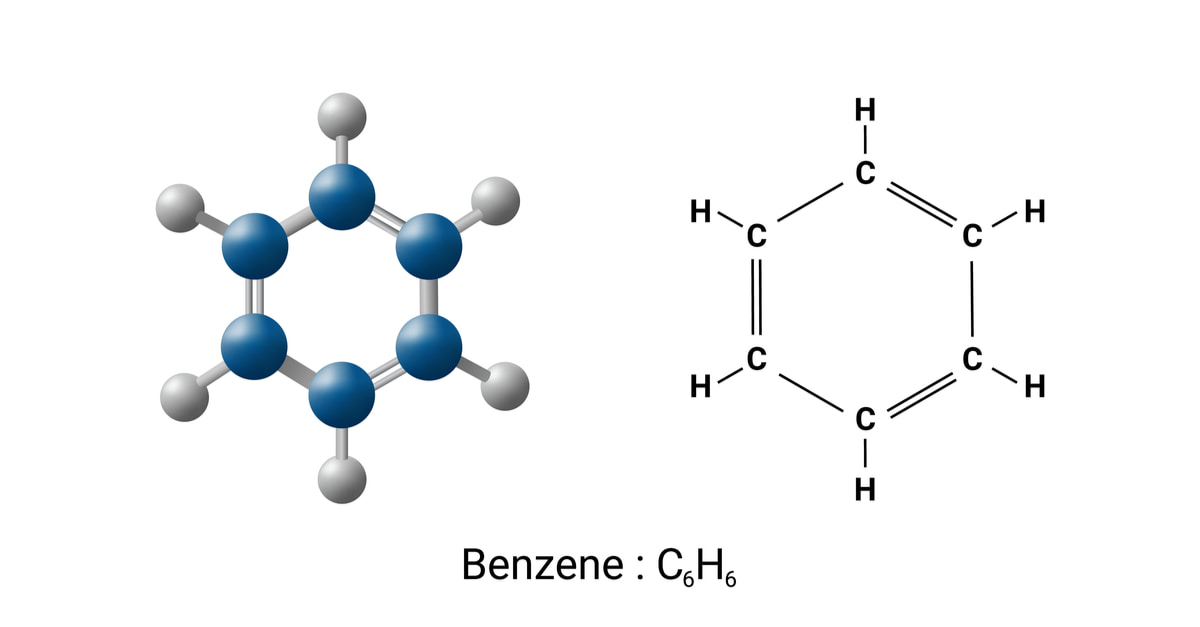
Benzen (C6H6) được biết đến như một hydrocarbon thơm với nhiều ứng dụng trong ngành công nghiệp và cuộc sống. Không chỉ vậy, benzen cũng là một dung môi hữu cơ thường được sử dụng. Nó có một cấu trúc khác với metan, ethylene hoặc acetylene. Vậy cấu trúc phân tử của benzen là gì? Các tính chất vật lý và hóa học của benzen là gì? Hãy cùng nhau tìm hiểu chúng trong bài viết hôm nay!
- Các phần mềm và website học toán lớp 1 nâng cao online hiệu quả nhất giúp trẻ phát huy toàn diện
- Những cách dạy trẻ 2 tuổi tập trung và phát triển toàn diện dễ thực hiện nhưng vẫn mang lại hiệu quả cao
- Thì tương lai hoàn thành: Chi tiết lý thuyết và bài tập có lời giải
- Bơi tiếng Anh là gì? Từ vựng và mẫu câu về bơi lộ trong tiếng Anh
- Mầm non bài tập Toán cho trẻ 5 tuổi – 11 dạng bài tập bổ trợ con tốt nhất
Khái niệm về benzen là gì?
Benzen là một hydrocarbon thơm ít hòa tan trong nước nhưng dễ dàng hòa tan trong dầu khoáng, dầu động vật và động vật, dung môi hữu cơ, v.v.
Trong công nghiệp, benzen là một vật liệu được sử dụng để tổng hợp nhiều hợp chất hữu cơ như anilin, clo benzen, nitrobenzene, phenol, … được sử dụng làm dung môi để hòa tan chất béo.
Kể từ những năm 1970, benzen đã bị hạn chế trong sử dụng công nghiệp. Tại Việt Nam, lệnh cấm sử dụng hóa chất benzen trong ngành đã được chỉ định ở mức 108 lb/qd.
Công thức phân tử của benzen là: C6H6.
- Khối lượng phân tử: 78
- Cấu trúc phân tử:
.jpg)
Công thức chung của benzen
Nhìn chung, benzen có công thức phân tử C6H6. Công thức chung của benzen và tính đồng nhất của nó là CNH2N-6 (N ≥ 6).
Cấu trúc phân tử của benzen
Benzen là một hydrocarbon thơm với 6 nguyên tử carbon được liên kết với nhau để tạo thành một vòng phẳng. Mỗi nguyên tử carbon trong benzen được liên kết với một nguyên tử hydro. Các liên kết trong cấu trúc vòng benzen là tất cả các liên kết cộng hóa trị. Đồng thời, vòng benzen có cấu trúc đối xứng.
Benzen và đồng tính luyến ái
Benzen là hydrocarbon thơm đơn giản nhất. Đồng tính luyến ái của Benzen là hydrocarbon thơm tương tự như benzen nhưng có hơn 6 nguyên tử carbon. Ví dụ: Toluen (C7H8), Ethylbenzen (C8H10), Xilen (C8H10), …
Cách đặt tên tên (danh pháp) là đẳng cấu, đồng phân của benzen
1. Đối với sự đồng nhất của benzen: Gọi tên ban đầu ankyl + benzen.
Ví dụ:
- C6H5CH3: Ethylbenzen
- C6H5CH2CH3: N-propylbenzen
- C6H5CH (CH3) 2: Isopropylbenzen
2. Gọi các đồng phân của benzen: dựa trên vị trí của các nhóm trên vòng benzen, chúng ta có tiền tố:
- O-: ortho (1,2)
- M-: Meta (1,3)
- P-: para (1,4)
Ví dụ: C6H4 (CH3) 2: Xilen
- O-Xilen (1,2-Dimethylbenzen)
- M-Xilen (1,3-Dimethylbenzen)
- P-Xilen (1,4-Dimethylbenzen)
Để làm bài tập về nhà tốt hơn, chỉ cần biết về cấu trúc benzen là không đủ, bạn cần biết thêm về bản chất của benzen từ vật lý đến hóa học.
Tính chất vật lý của benzen
Benzen (C6H6) là một chất lỏng không màu, nhẹ hơn nước và không hòa tan trong nước. Benzen có thể hòa tan nhiều chất như dầu nấu, cao su, nến, iốt … và nhiều dung môi hữu cơ khác. Benzen là độc hại và dễ cháy.
C6H6 có mật độ 0,8786 g/cm3 chất lỏng, nóng chảy ở 5,5 độ C, sôi ở 80,1 độ C. (Wikipedia)
Tính chất hóa học của benzen
Các tính chất của benzen có các phản ứng hóa học điển hình như lửa, vì vậy và cộng. C6H6 có cả phản ứng và phản ứng cộng, nhưng phản ứng cộng khó hơn C2H4 và C2H2.

Benzen dễ cháy
Giống như các hydrocacbon khác, đốt cháy oxy để tạo ra CO2 và hơi nước. Tuy nhiên, khi benzen cháy trong không khí, ngoài CO2 và hơi nước cũng tạo ra bồ hóng.
2C6H6 + 15O2 (nhiệt độ) → 12CO2 + 6H2O
Phản ứng của Benzen đối với brom (phản ứng)
Đặc điểm cấu trúc của benzen: Khi làm nóng hỗn hợp benzen bằng brom, bột sắt có màu nâu đỏ của brom và có khí hido bromide bay ra.

C6H6 (L) + BR2 (L) (T, Bột Fe) → C6H5BR (chất lỏng không màu) + HBR (K)
Trong phản ứng trên, nguyên tử hydro trong phân tử benzen được thay thế bằng nguyên tử brom.
Phản ứng cộng của Benzen
Benzen không phản ứng với dung dịch BR2, chứng minh rằng benzen rất khó tham gia vào các phản ứng cộng như C2H4 và C2H2. Tuy nhiên, ở nhiệt độ và chất xúc tác thích hợp, C6H6 tham gia vào phản ứng cộng với một số chất, chẳng hạn như H2, …
C6H6 + 3H2 (T, NI) → C6H12
|
Xây dựng một nền tảng toán học vững chắc cho trẻ em từ khi còn nhỏ với đa phương tiện, cực kỳ rẻ có giá dưới 2k/ngày với toán học khỉ.
|
Làm thế nào để chuẩn bị benzen?
Trong cuộc sống, benzen được sử dụng rất nhiều trong sản xuất dược phẩm hoặc các chất quan trọng để phục vụ nhu cầu của người dân. Vậy benzen được chuẩn bị như thế nào? Vui lòng tham khảo sử dụng sau:
Phản ứng trùng hợp xảy ra khi chất xúc tác C và được làm nóng ở nhiệt độ 600 độ C.
3Ch = Ch → C6H6
C6H5COOH + NaOH → C6H6 + NA2CO3
C6H12 → C6H6 + 3H2
C6H14 → C6H6 + 4H2
Xem thêm:
Ứng dụng của benzen
Xem thêm : Cùng bé học toán lớp 2 mét đơn giản nhờ 5+ kinh nghiệm này!
Trong ngành công nghiệp, benzen được sử dụng trong một số ngành công nghiệp hữu cơ. Bên cạnh đó, chúng cũng được sử dụng để tổng hợp các monome trong việc sản xuất polyme cho nhựa, cao su và sợi.
.jpg)
Benzen cũng thường được sử dụng làm dung môi để hòa tan các chất như dầu mỡ, cao su và vecni. Được sử dụng để loại bỏ dầu mỡ cho xương, sợi, vải, len, nỉ, giặt khô, loại bỏ dầu mỡ cho các tấm kim loại. Ngoài ra, các công cụ với dầu mỡ thường sử dụng benzen để làm sạch.
Benzen cũng được sử dụng để tạo ra các chất trong sản xuất như nitrobenzene, aniline, phenol, tổng hợp thuốc nhuộm, dược phẩm, thuốc trừ sâu, cumene, acetone và phenol.
Là benzen có độc không? Nó ảnh hưởng đến sức khỏe con người như thế nào?
Ngoài những tác động lớn ở trên, benzen còn được gọi là một chất rất độc hại cho sức khỏe của chúng và khả năng gây ung thư là rất cao. Những người bị ngộ độc benzen cấp tính sẽ trải qua các triệu chứng sau:
.jpg)
-
Nhức đầu, chóng mặt, buồn nôn, nhầm lẫn.
-
Mất ý thức, hôn mê, mất trí nhớ.
-
Mất thính giác.
-
Viêm phổi.
-
Bỏng, viêm kết mạc, giác mạc, mù màu.
-
Viêm gan nhiễm độc.
-
Viêm cầu thận.
-
Tổn thương tim mạch
Khi ngộ độc mãn tính sẽ có 2 giai đoạn chính. Đó là:
-
Giai đoạn khởi phát khiến chúng ta mắc chứng rối loạn tiêu hóa, rối loạn thần kinh, rối loạn huyết học.
-
Trong giai đoạn toan phat sẽ xuất hiện các triệu chứng như chảy máu, thiếu máu, bệnh bạch cầu, …
Chúng ta có thể bị đầu độc bởi benzen thông qua các dòng sau:
-
Trong thực phẩm, benzen được sử dụng để bảo quản thực phẩm, đặc biệt là nước ngọt đóng chai.
-
Benzen ở trong không khí khi chúng ta sử dụng để sản xuất công nghiệp tại thời điểm đó, khí sẽ bay hơi. Hoặc trong sự lãng phí các phương tiện vận chuyển nhiên liệu hóa thạch.
Đối với nhân viên khai thác dầu mỏ, công nhân sản xuất nhựa, công nhân sản xuất và chế biến nhựa, … Để đảm bảo sức khỏe, bạn nên gặp bác sĩ thường xuyên, định kỳ 6 tháng nên tổ chức kiểm tra một lần. Nếu được phát hiện ngay cả khi chỉ tìm thấy một trường hợp ngộ độc, cần phải tổ chức kiểm tra tất cả các công nhân tiếp xúc. Về các hiện tượng lâm sàng, chú ý đến tình trạng cơ thể: cân nặng, ăn uống, ngủ … Ngoài ra, cần phải phát hiện các dấu hiệu chảy máu.
Tập thể dục trên Benzen SGK Hóa học 9 với các giải pháp
Dựa trên kiến thức trên, bạn có thể tận dụng để giải quyết một số bài tập trong sách giáo khoa hóa học lớp 9:

Bài tập 1 (trang 125 Hóa học SGK 9)
Cấu trúc đặc biệt của phân tử benzen là:
a) Phân tử có 6 mặt.
B) Phân tử có ba liên kết đôi.
C) Phân tử có 6 cạnh chứa ba liên kết đôi xen kẽ ba liên kết đơn.
D) Phân tử có 6 cạnh chứa ba liên kết kép và ba liên kết đơn.
Chọn câu tốt nhất trong các câu trên.
Đề xuất cho câu trả lời:
Chọn Câu hỏi C) Đúng.
Bài tập 2 (trang 125 SGK)
Một số sinh viên viết công thức cấu trúc của benzen như sau:

Xin vui lòng cho biết công thức nào là chính xác, sai, tại sao?
Đề xuất cho câu trả lời:
Công thức cấu trúc chính xác của benzen: b), d), e)
(a) sai vì 2 liên kết PI trong hai nguyên tử C liền kề (sai về vị trí của liên kết đôi)
Xem thêm : Tìm hiểu 1 ki lô mét vuông bằng bao nhiêu hecta?
(c) sai vì có 5 nguyên tử C
Bài tập 3 (trang 125 SGK)
Hãy để benzen hành động với brom để tạo ra brombenzene:
a) Viết một phương trình hóa học (chỉ định các điều kiện phản ứng).
b) Tính khối lượng benzen cần thiết để chuẩn bị 15,7g brombenzene. Biết hiệu quả phản ứng đạt 80%.
Đề xuất cho câu trả lời:
A) Phương trình phản ứng:
C6H6 + BR2 (Fe) → C6H5BR + HBr.
b) NC6H5BR = 15,7 / 157 = 0,1 mol.
Theo phương trình: NC6H6 = NC6H5BR = 0,1 mol.
Làm h = 80% nên:
MC6H6 = 0,1. 78: 80% = 9,75 (g)
Bài tập 4 (trang 125 SGK)
Vui lòng chỉ ra những chất nào trong các chất sau đây có thể làm mất màu dung dịch brom. Giải thích và viết phương trình hóa học (nếu có).
a) C6H6.
B) CH2 = CH – CH = CH2.
C) CH3 – C.
D) CH3 – CH3.
Đề xuất cho câu trả lời:
Chỉ chất B) và C) Dispolor Brom Dung dịch. Bởi vì trong các phân tử có liên kết kép và liên kết liên kết tương tự như C2H4 và C2H2.
B) CH2 = CH – CH = CH2 + 2BR2 (dd) → CH2BR – CHBR – CHBR – CH2BR.
Hoặc: CH2 = CH – CH = CH2 + BR2 → CH2BR – CHBR – CH = CH2
C) CH3 – C ≡ CH + 2BR2 → CH3 – CBR2 – CHBR2
Hoặc CH3 – C ≡ CH + BR2 → CH3 – CBR = CHBR
Tập thể dục về hóa chất benzen để học sinh tự đào tạo
Bài 1: Điều nào sau đây có khả năng tham gia vào sự trùng hợp polymer?
A. Benzen B. Toluene C. 3 Propane D. Stiren
Bài 2: Chất nào sau đây làm mất màu dung dịch KMNO4 ở nhiệt độ bình thường?
A. Benzen B. Toluene C. Propane D. Stiren
Bài 3: Benzen hoạt động với BR2 theo tỷ lệ mol là 1: 1 (mặt bột FE), các sản phẩm hữu cơ thu được là
A.C6H6BR2 B. C6H6BR6
C. C6H5BR D. C6H6BR4
Bài học 4: Benzen hoạt động với H2 còn lại với bột xúc tác, thu được
A. Hex-1-en B. Hexane
C. 3 Hex-1-in D. Xiclohexan
Bài học 5: Phản ứng benzen với clo tạo ra C6H6Cl6 xảy ra theo:
A. Có bột Fe xúc tác B. Có ánh sáng khuếch tán
C. dung môi nước D. với dung môi CCL4
Bài 6: Trình tự bao gồm các nhóm làm cho vòng tròn benzen dễ dàng hơn và ưu tiên vị trí m- IS:
A. -cnh2n+1, -oh, -nh2 B.THERch3, -NH2, -no2
C.
Bài 7: Phản ứng nào sau đây không xảy ra:
A. Benzen + CL2 (AS) B.Benzene + H2 (Ni, Tº)
C. Benzen + BR2 (DD) D.Benzen + HNO3 /H2SO4 (d)
Bài học 8: Đặt benzen + cl2 (as) Chúng ta có được dẫn xuất clo A. Vì vậy, A là:
A.C6H5CL BP-C6H4CL2 C.C6H6CL6 DM-C6H4CL2
Bài 9: Hãy để benzen hoạt động với lượng HNO3 tập trung với các chất xúc tác H2SO4 tập trung để chuẩn bị nitrobenzen. Khối lượng nitrobenzen được điều chế từ 19,5 tấn benzen (hiệu suất phản ứng 80%) là bao nhiêu?
Bài 10: Chất x là tính đồng nhất của benzen, công thức đơn giản nhất là C3H8. Công thức phân tử của X là gì?
Bài 11: Đốt cháy hoàn toàn Ankybenzen X thu được 7,84 lít CO2 (DKTC) và 3,6 gram H2O. Công thức phân tử của X là gì?
Con khỉ ở trên đã giới thiệu cho bạn các tính chất vật lý, tính chất hóa học, cấu trúc phân tử của benzen C6H6. Hy vọng rằng bài viết này sẽ giúp bạn hiểu rõ hơn. Nếu bạn cần tìm hiểu thêm về nhiều chủ đề khác, bạn có thể truy cập trang web để có kiến thức thú vị hơn!
Nguồn: https://truongnguyentatthanh.edu.vn
Danh mục: Giáo dục




![[GIẢI ĐÁP] Chứng chỉ IELTS có được miễn thi tốt nghiệp không?](https://truongnguyentatthanh.edu.vn/wp-content/uploads/GIAI-DAP-Chung-chi-IELTS-co-duoc-mien-thi-tot-800x450.jpg)

